研究契約 4 種 — Loan Agreement / Master Research / Collaboration / IPA + 法規制 (FDA/510K/薬機法/公正取引)
Manabe-san が KOL 施設に WIP/Prototype を提供する際の **法的枠組み** を 6 sections で完全可視化。**FDA 510(k) + 日本薬機法 + 公正取引** の 3 法規制下で **LA (Loan Agreement) / MRA (Master Research Agreement) / CA (Collaboration Agreement) / IPA (Internal Project Agreement)** を使い分け、研究と販売を厳格分離。
TL;DR
- 3 法規制: FDA 510(k) (米国医療機器承認) / 日本薬機法 (旧薬事法) / 公正取引 (日本では 1 年ずつ更新が原則)
- 4 契約種類: LA (装置・WIP 一時貸与) / MRA (master 包括契約) / CA (個別 collaboration) / IPA (内部 project 単位)
- 典型 timeline: 提案 → 法務 review (4w) → 契約案 (2w) → サイン (1w) → 提供 (1-2w) ≈ 8-12 weeks。緊急短縮は exception
013 法規制 — FDA 510(k) / 日本薬機法 / 公正取引
WIP/C2P を取り巻く法的枠組み、医療機器メーカーの遵守義務。
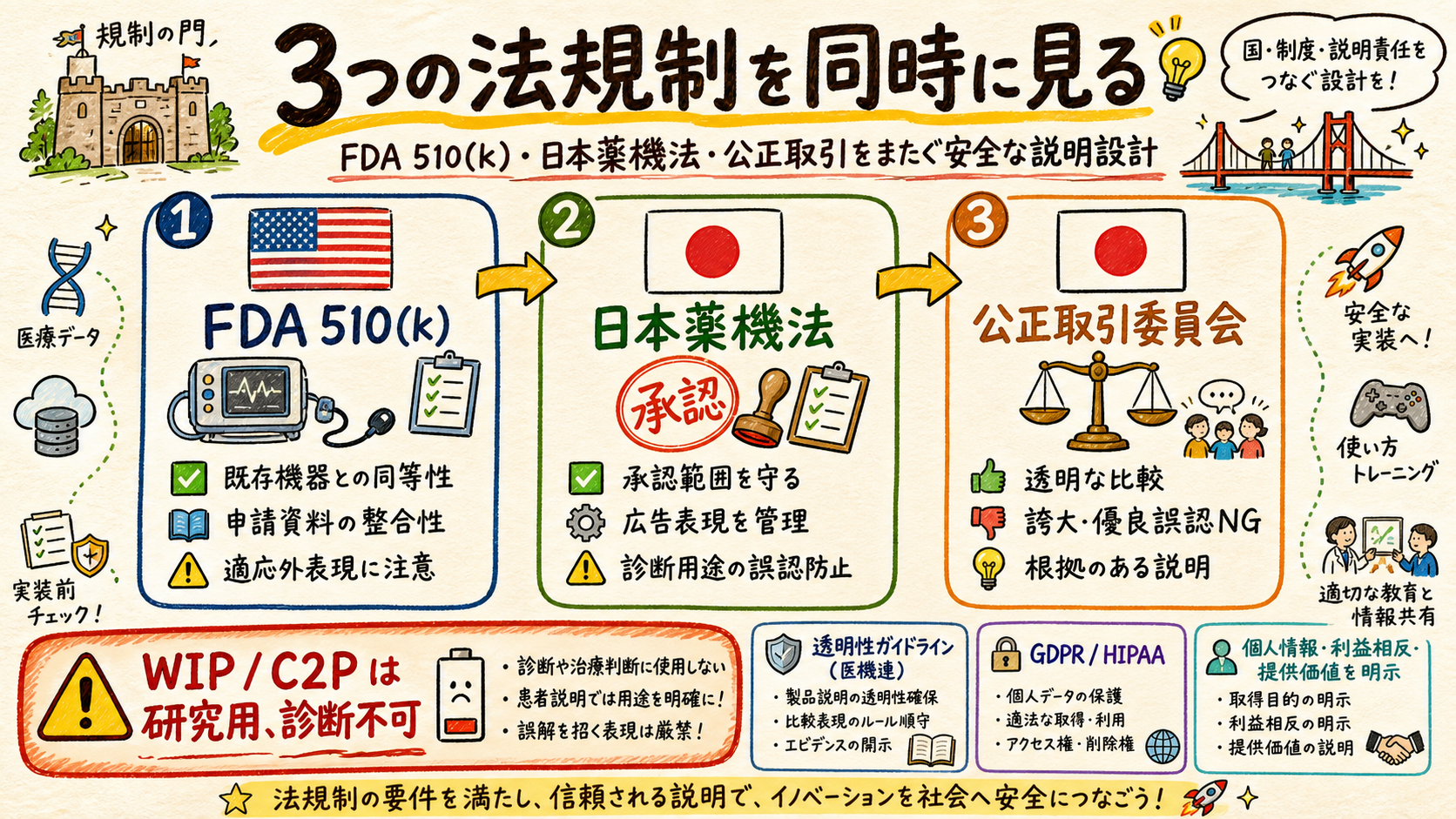
| 法規制 | 国/領域 | WIP/C2P への影響 |
|---|---|---|
| FDA 510(k) | 米国 | 医療機器承認 process、未取得 sequence は診断不可 |
| 薬機法 (旧薬事法) | 日本 | 医療機器販売前の承認、研究用 WIP は対象外 |
| 公正取引 (独禁法) | 日本 | 研究と販売の分離、贈与・接待上限 |
| 透明性ガイドライン | 日本 (業界自主規制) | 医師への金銭・物品の公開義務 |
| GDPR / HIPAA | EU / 米国 | 患者データ取扱い (国際 collaboration 時) |
📚 用語解説 — FDA 510(k): 米国 FDA の医療機器承認 process。「既存類似機器との実質的同等性 (substantial equivalence)」を示す書類提出。承認後 K xxxxxx 番号付与、医療機器として販売可能。
📚 用語解説 — 薬機法 (医薬品医療機器等法): 旧薬事法 (2014 改名)。日本の医薬品・医療機器の品質・有効性・安全性を確保。クラス I (低リスク) → IV (高リスク) で承認 process が異なる。
📚 用語解説 — 公正取引委員会: 独占禁止法 + 景品表示法を執行。医療機器メーカーは「研究と販売の分離」「贈与・接待 (5 万円程度上限) の透明化」を監視。
🛠️ 運用方法: (1) 提案資料に「WIP = FDA/薬機法 未取得」「研究用、診断不可」明示 (2) 国際 collaboration では GDPR (EU) / HIPAA (米国) 患者データ取扱い確認 (3) 透明性ガイドライン公開対象であれば事前に医師同意 (4) Common Limit page にリンク参照、毎回詳細書かない
⚠️ アンチパターン: 「FDA 取得済」を自分で誇示 → メーカー責任、Sales 経由必須。WIP を「医療機器」と呼ぶ → 薬機法違反、研究用と明示。透明性ガイドライン公開を skip → 公取委から指摘リスク。
02LA (Loan Agreement) — 装置・WIP 一時貸与契約
短期貸与、研究目的限定、返却義務付き。
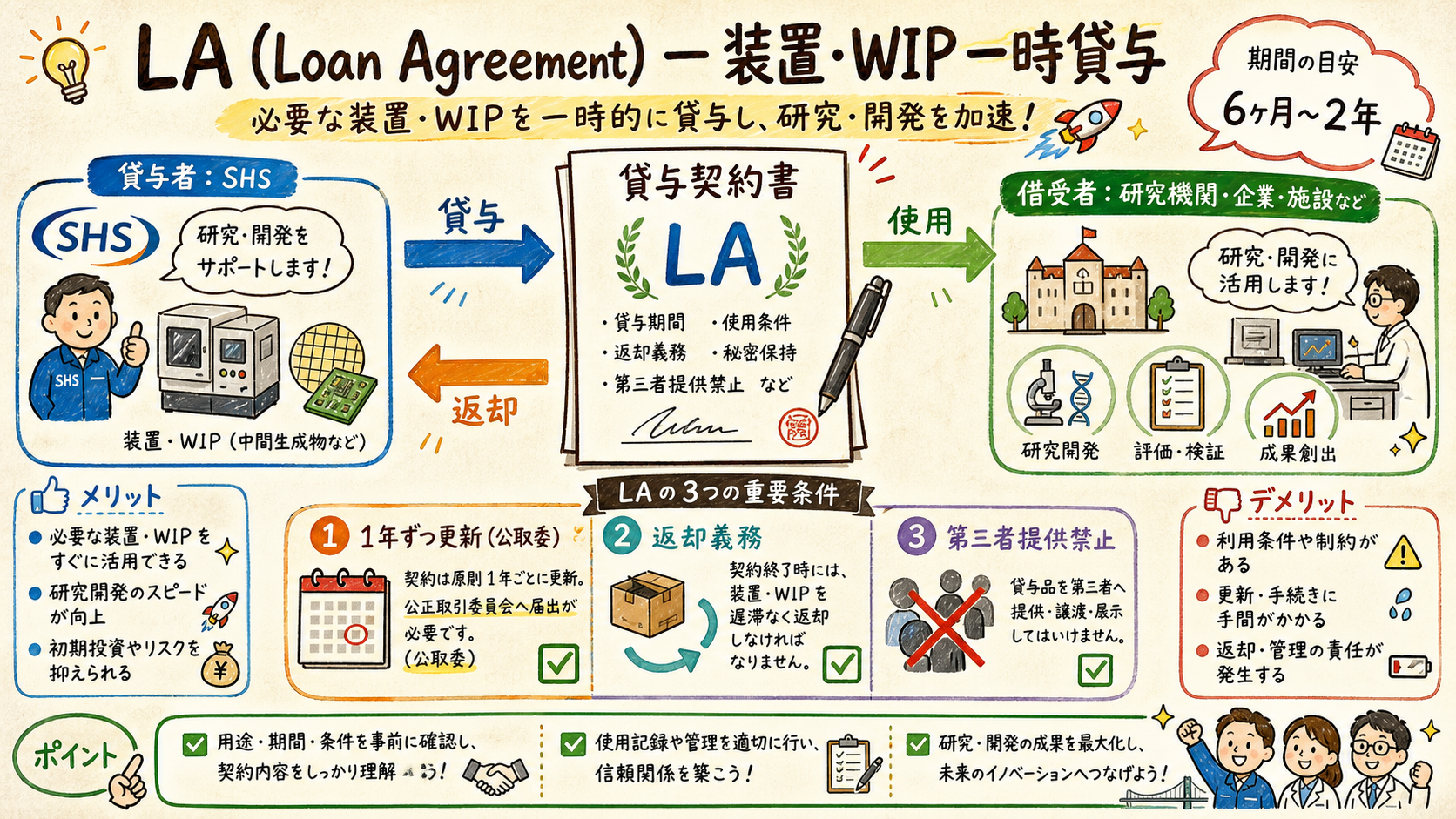
| LA 構成要素 | 内容 | 典型期間 |
|---|---|---|
| 対象資産 | 装置 / WIP / Prototype 部品 | 案件次第 |
| 貸与目的 | 研究 / 評価 / 学会発表のみ | (契約全期間) |
| 貸与期間 | 典型 6 ヶ月〜2 年 | 更新可 |
| 返却義務 | 契約終了時に原状返却 | — |
| 第三者提供禁止 | 絶対禁止 | — |
| 公正取引 (日本) | 1 年ずつ更新が原則 | — |
📚 用語解説 — Loan Agreement (LA): 装置や WIP を一時貸与する契約。所有権はメーカー保持、施設は使用権のみ。「無償貸与」と「有償貸与」あり、研究 LA は通常無償。
📚 用語解説 — 公正取引 1 年ずつ更新: 日本の独禁法・公正取引慣習で、無償貸与は 原則 1 年ごと更新。長期固定は「実質贈与」と見なされるリスク、毎年 review が transparency 維持。
📚 用語解説 — 第三者提供禁止: 借りた WIP を別施設・別研究者に提供するのは絶対禁止 (knowledge transfer も含む)。Cross-WIP discipline と関連。
🛠️ 運用方法: (1) LA は IPA より軽量、単発 WIP 提供で活用 (2) 1 年ずつ更新を契約に明記、長期固定回避 (3) 装置貸与時は IT 部門と引取 / 返却 logistics 調整 (4) 第三者提供禁止を医師に明示 (4 法務 review 4 weeks 程度を見込む
⚠️ アンチパターン: LA の無期限 / 自動更新 → 公取委から指摘、毎年 review 必須。借りた WIP を別施設に提供 → 契約違反、信頼喪失。返却 logistics を施設任せ → 紛失リスク、SHS で管理。
03MRA (Master Research Agreement) — 包括契約
複数案件・長期 collaboration の master 契約、個別案件は SOW で追加。
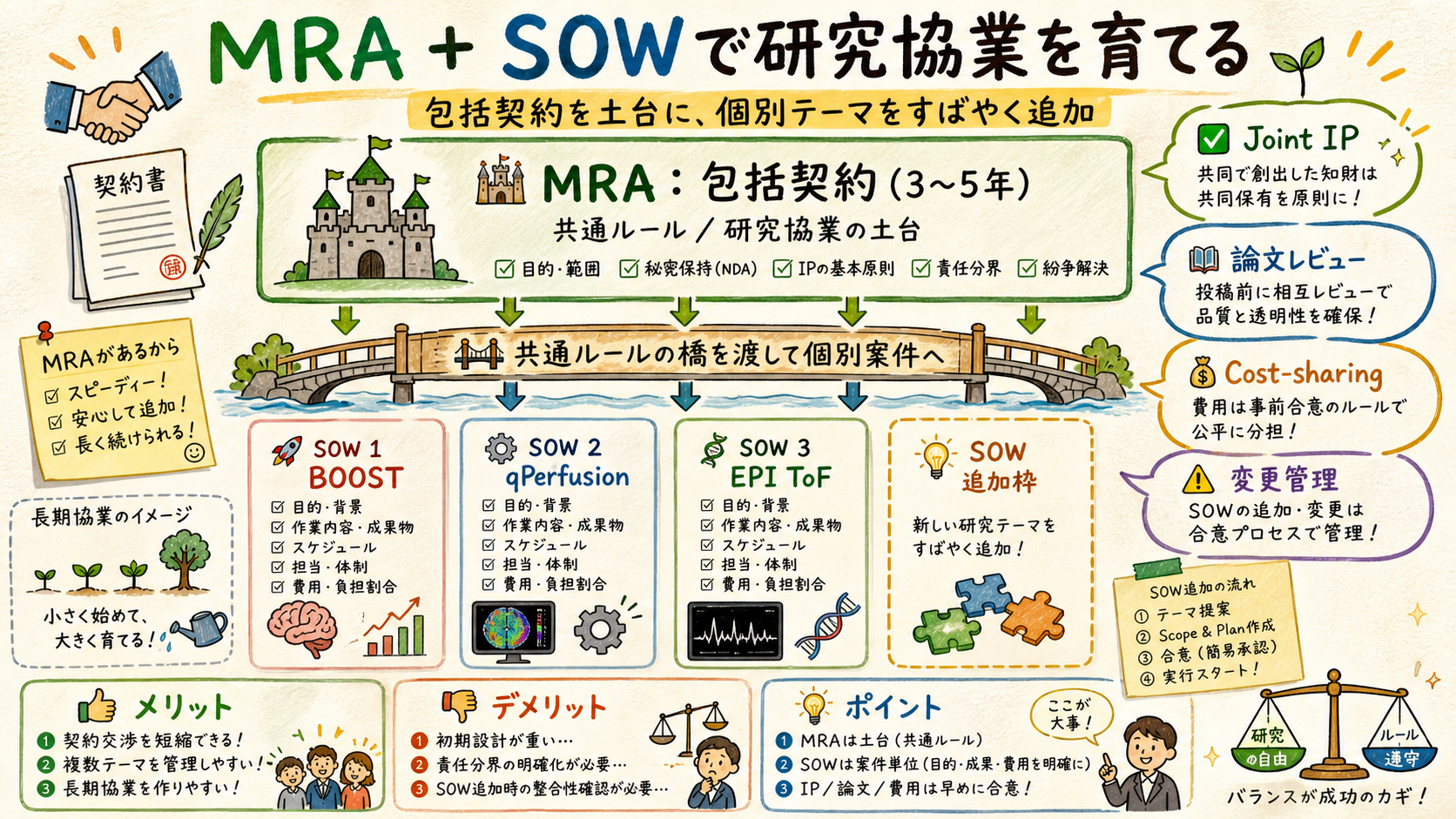
| MRA 構成要素 | 内容 |
|---|---|
| 有効期間 | 典型 3-5 年 (long term) |
| 対象範囲 | 複数領域 (Cardiac + Neuro + Body 等) |
| 個別案件 | SOW (Statement of Work) で追加 |
| IP (知的財産) | Joint IP / 各社 IP の取扱い明示 |
| 論文発表 | 両社事前 review / 共著 / acknowledgment |
| 費用負担 | Cost-sharing / Sponsored research の選択 |
📚 用語解説 — MRA (Master Research Agreement): 大学・研究機関と SHS 間の包括契約。1 度締結で複数案件 SOW 追加可能、個別案件ごとの法務負担軽減。
📚 用語解説 — SOW (Statement of Work): 個別案件の詳細仕様書 (目的 / 期間 / 成果物 / 費用 / 担当者 等)。MRA 配下で迅速締結。
📚 用語解説 — Joint IP: 共同研究で生まれた知的財産の取扱い。事前合意: 「両社共有」「発明者所属機関」「特許化決定権」等。
🛠️ 運用方法: (1) 複数案件想定 KOL は MRA 締結を提案 (NCVC, 三重大, 京大等) (2) SOW で個別 sequence を追加 (BOOST + qPerfusion + EPI ToF 等) (3) IP 取扱いは法務 + 産学連携室と事前合意 (4) 論文発表は両社 review 経由
⚠️ アンチパターン: SOW なしで研究開始 → 範囲曖昧、後で disagreement。Joint IP 取扱い skip → 特許化時に紛争。論文 review skip → 機密情報誤公開リスク。
04CA (Collaboration Agreement) — 個別 collaboration 契約
MRA なしで単発 collaboration、IPA より軽量、LA より柔軟。
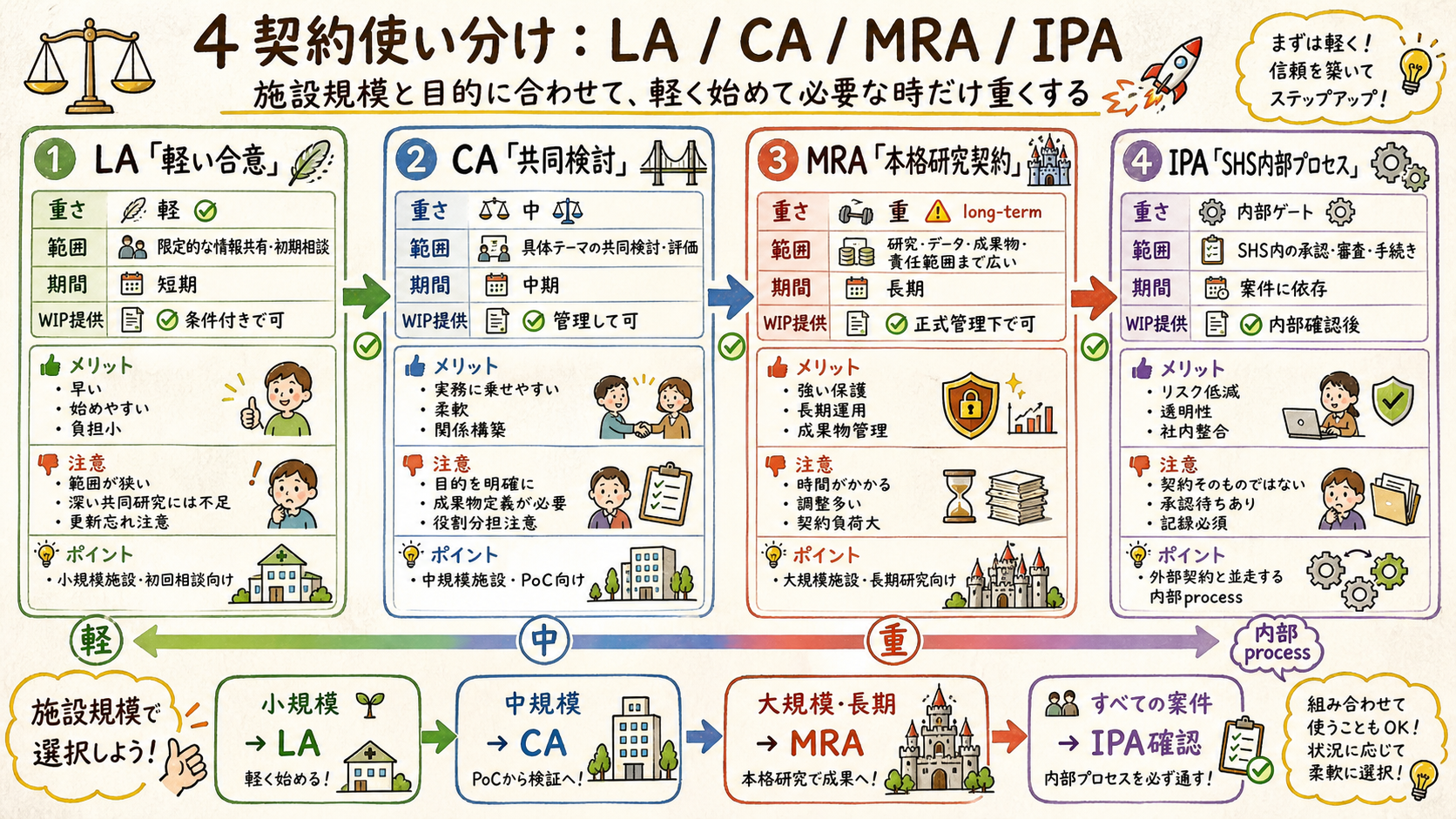
| 契約タイプ | 範囲 | 期間 | 重さ | WIP 提供 |
|---|---|---|---|---|
| LA | 単発 WIP 貸与 | 6 ヶ月〜2 年 | 軽 | OK |
| CA | 単発 collaboration | 1-2 年 | 中 | OK |
| MRA + SOW | 包括 + 複数案件 | 3-5 年 | 重 | OK |
| IPA | Internal Project Agreement | 案件次第 | 中-重 | OK (社内 process) |
📚 用語解説 — Collaboration Agreement (CA): 単発の研究 collaboration 契約。MRA がない施設や、新規 collaboration の試行段階で使用。論文発表 + IP + 費用負担の最小限合意。
📚 用語解説 — IPA (Internal Project Agreement): SHS 内部の project 単位契約 (社内 process)。法務契約と分離、社内決裁・予算 allocation・担当者 assign のため。
📚 用語解説 — 4 契約の使い分け: 装置貸与だけ = LA / 単発 collab = CA / 長期 + 複数案件 = MRA + SOW / 全件 SHS 内部承認 = IPA (上記と並行)。
🛠️ 運用方法: (1) 施設の collaboration 規模で 4 契約から選択 (2) 新規施設は CA で試行、成功なら MRA に格上げ (3) IPA は SHS 内部で必ず先行締結 (4) 4 契約とも法務 review + 公取委 / 透明性ガイドライン 遵守確認
⚠️ アンチパターン: CA で済ませて MRA 締結を先延ばし → 案件増加で個別契約コスト膨張。IPA を skip して直接 LA/CA → SHS 内部承認なしで進行、後で予算 / 担当 issue。
05典型 timeline 8-12 weeks + 法務 review process
提案 → 法務 4w → 契約案 2w → サイン 1w → 提供 1-2w、緊急短縮は exception。
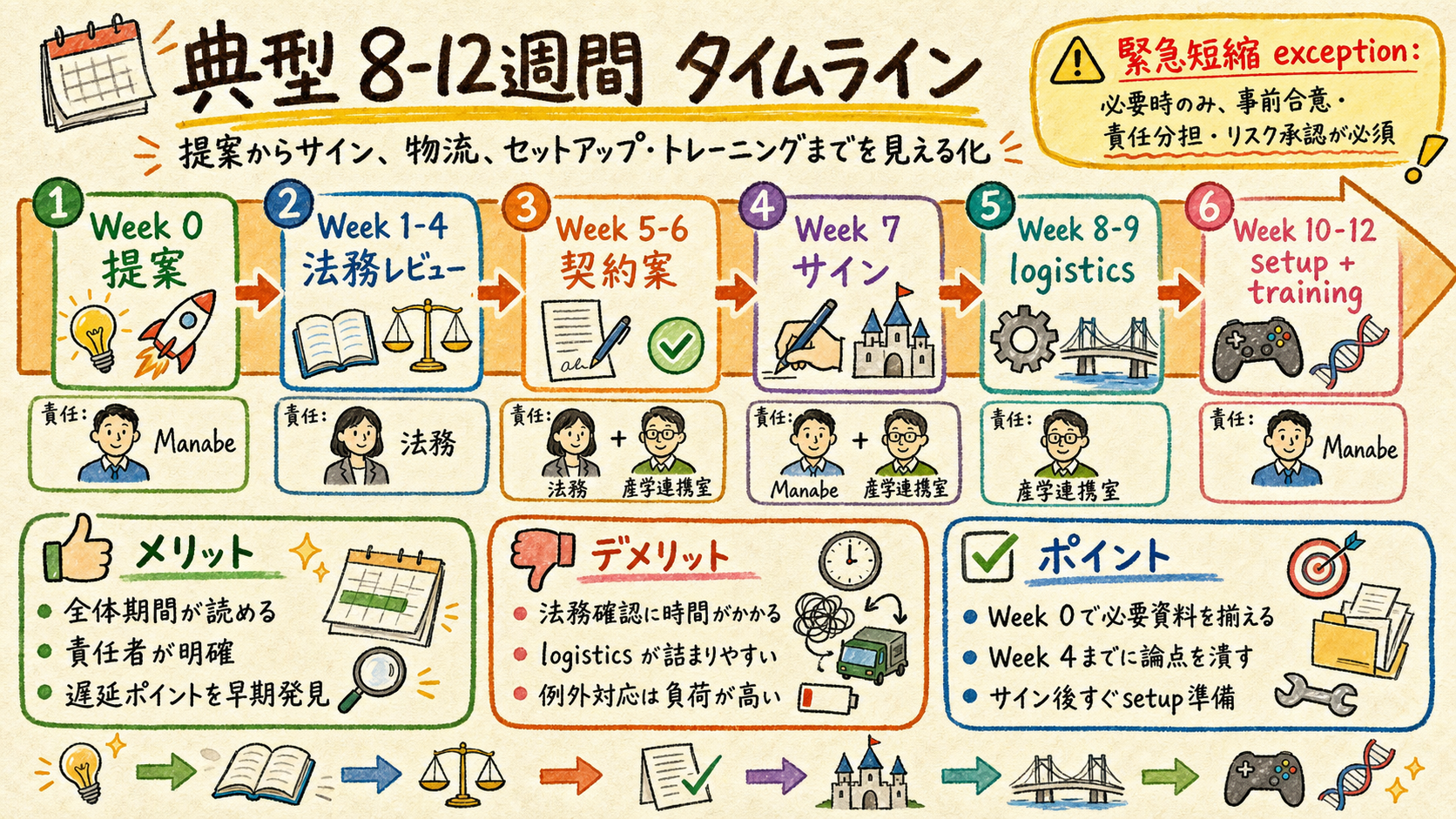
- Week 0: Manabe (R&C) が KOL に Prototype 提案、医師 + IT + 法務担当に紹介
- Week 1-4: SHS 法務 + 施設法務 で契約条項 review (LA/CA/MRA + IPA 並行)
- Week 5-6: 契約案 ドラフト → 両者 review → 修正
- Week 7: 双方サイン (代表者 / 産学連携室 / R&C 部長)
- Week 8-9: WIP / 装置 logistics → 施設受領 → IT インストール
- Week 10-12: 初期 setup + Scientist による installation 確認 + 技師 training
📚 用語解説 — 法務 review: SHS Japan 法務 + 施設の産学連携室 / 法務担当。両者で条項 review、典型 4 weeks。
📚 用語解説 — 産学連携室: 大学に通常設置されている、企業との共同研究を統括する部署 (TLO 含む場合あり)。
📚 用語解説 — 緊急短縮 exception: 学会 deadline 等で緊急時は 4-6 weeks に短縮可能だが、法務リスク増、原則は 8-12 weeks。
🛠️ 運用方法: (1) 訪問時に「8-12 weeks タイムライン」を医師に明示、意欲が冷めない調整 (2) 学会発表 deadline がある場合は 16+ weeks 前に提案開始 (3) 産学連携室 / 法務担当を早期 introduce (4) IPA を SHS 内部で並行進行 (week 0-4)
⚠️ アンチパターン: 8-12 weeks を約束せず曖昧 → 医師の意欲冷却。学会 deadline 直前に提案 → 緊急短縮 exception 連発で法務に負担。IPA 並行進行を skip → 契約締結時に SHS 内部予算 / 担当が決まっていない。
06公正取引 1 年ずつ更新 + 透明性ガイドライン
日本特有の規制、無償貸与は 1 年更新、医師への支払いは公開。
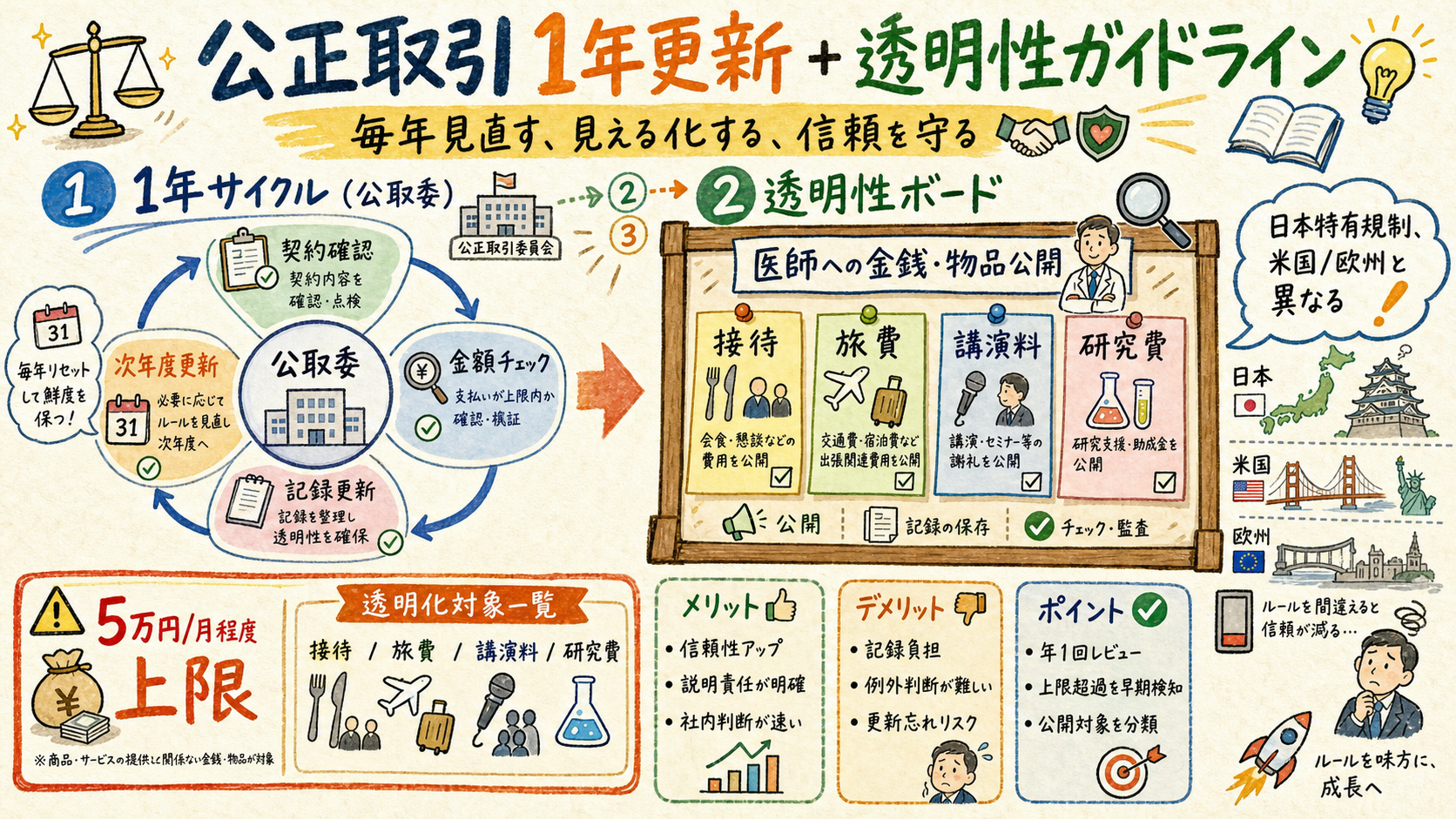
| 項目 | 対象 | 規制 | 公開 |
|---|---|---|---|
| 無償 LA / WIP | 装置・sequence 貸与 | 1 年ずつ更新 | — |
| 研究費 / 委託費 | 施設への金銭 | 上限 / 必要性 | 透明性 GL で公開 |
| 旅費 (学会招待) | 医師への旅費 | 上限 / 公益性 | 透明性 GL で公開 |
| 接待 / 贈与 | 食事・物品 | 5 万円 / 月 程度上限 | 透明性 GL で公開 |
| 講演料 / 顧問料 | 医師への報酬 | 上限 / 必要性 | 透明性 GL で公開 |
📚 用語解説 — 1 年ずつ更新: 公正取引委員会 + 独禁法慣習。長期固定の無償貸与は「実質贈与」と見なされるリスク、毎年 review で透明性維持。
📚 用語解説 — 透明性ガイドライン: 日本医療機器産業連合会 (医機連) の自主規制。医師への金銭・物品供与の公開義務 + 上限、各社が web で年次公開。
📚 用語解説 — 5 万円 / 月 程度上限: 食事・物品の事実上上限、超過時は社内 escalation。学会期間中の懇親会等は別 category。
🛠️ 運用方法: (1) LA 締結時に「1 年ずつ更新」を契約に明記 (2) 研究費 / 旅費 / 接待 を Manabe 自身が記録、社内 transparency システムに入力 (3) 学会招待時の旅費は事前に医師合意 (4) 5 万円超過の食事は社内 escalation (5) 全件 透明性ガイドライン公開対象として整理
⚠️ アンチパターン: LA を多年固定 → 公取委指摘リスク。透明性ガイドライン公開対象を skip → 業界自主規制違反、社内処分。接待で 5 万円超過を無申告 → 透明性違反 + 公取委リスク。
結論
- 3 法規制: FDA 510(k) / 日本薬機法 / 公正取引 (独禁法 + 透明性ガイドライン)。WIP/C2P は研究用、診断不可。
- 4 契約種類使い分け: LA (装置貸与) / CA (単発 collab) / MRA + SOW (包括) / IPA (SHS 内部 process)。施設規模 + 案件特性で選択。
- 典型 8-12 weeks (緊急短縮 exception)、1 年ずつ更新 (公取委)、透明性ガイドライン公開義務。Common Limit page にリンク参照。